L’Inde se joindra aux essais cliniques du vaccin russe Spoutnik V
Russia Beyond désormais sur Telegram ! Pour recevoir nos articles directement sur votre appareil mobile, abonnez-vous gratuitement sur https://t.me/russiabeyond_fr
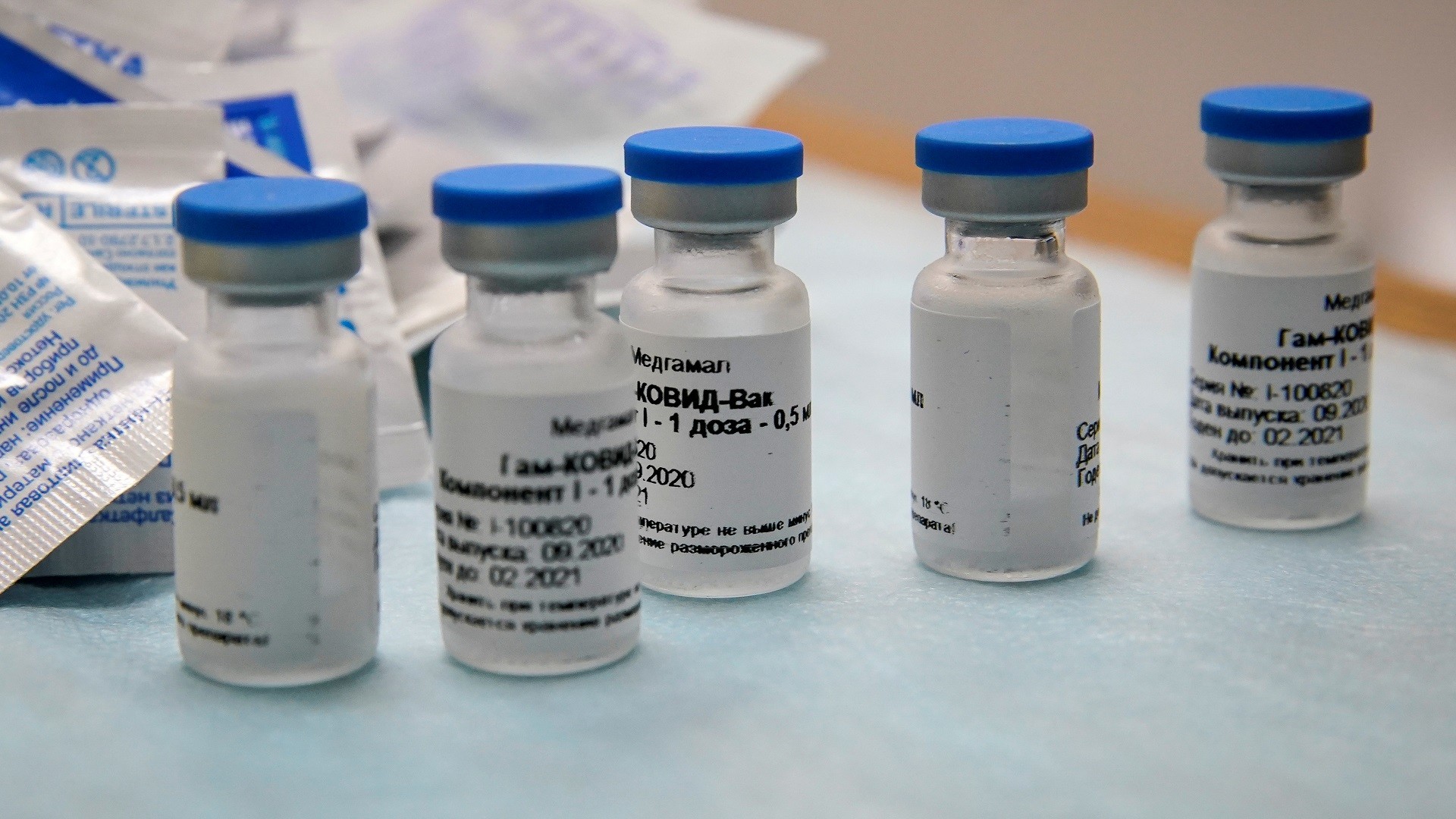
Le Contrôleur général des médicaments de l’Inde a autorisé le Fonds d’investissement direct russe (RDIF) et la compagnie pharmaceutique indienne Dr. Reddy’s Laboratories à conduire dans ce pays d’Asie les phases 2 et 3 des essais cliniques du vaccin russe Spoutnik V, développé contre la Covid-19, informe le site officiel dédié à ce préparatif.
C’est en septembre dernier que les deux structures s’étaient accordées pour cette opération conjointe, en vue de laquelle le RDIF s’est engagé à fournir à l’Inde 100 millions de doses du vaccin.
« Nous sommes heureux de notre collaboration avec les autorités de régulation indiennes et nous fournirons les données sur la sûreté et l'immunogénicité du vaccin obtenues au cours de la phase 3 des essais en Russie, en supplément des données des tests cliniques en Inde, pour faciliter la réussite des essais du Spoutnik V dans le pays », a commenté Kirill Dmitriev, directeur général du RDIF.
À noter que le Spoutnik V fait actuellement l’objet d’essais cliniques de phase 3 auprès de 40 000 volontaires en Russie. Il est également testé en Biélorussie, au Venezuela, ainsi qu’aux Émirats arabes unis.
Pour rappel, développé par l’Institut Gamaleïa, le Spoutnik V a été le premier vaccin anti-Covid-19 enregistré au monde, le 11 août. Depuis, un second préparatif d’élaboration nationale a reçu cette approbation du ministère russe de la Santé : l’EpiVacCorona, mis au point par le centre sibérien Vektor.
Dans cet autre article, nous vous résumons ce que l’on sait au sujet de ce deuxième vaccin.
Dans le cadre d'une utilisation des contenus de Russia Beyond, la mention des sources est obligatoire.
Abonnez-vous
gratuitement à notre newsletter!
Recevez le meilleur de nos publications directement dans votre messagerie.